药物临床试验机构
日期:2019-04-03 信息来源:
我院国家药物临床试验机构于2019年10月通过国家药品监督管理局(NMPA)资格认定,共批准6个专业,包括:呼吸内科、心血管内科、消化内科、妇科、泌尿外科和小儿(呼吸)专业。
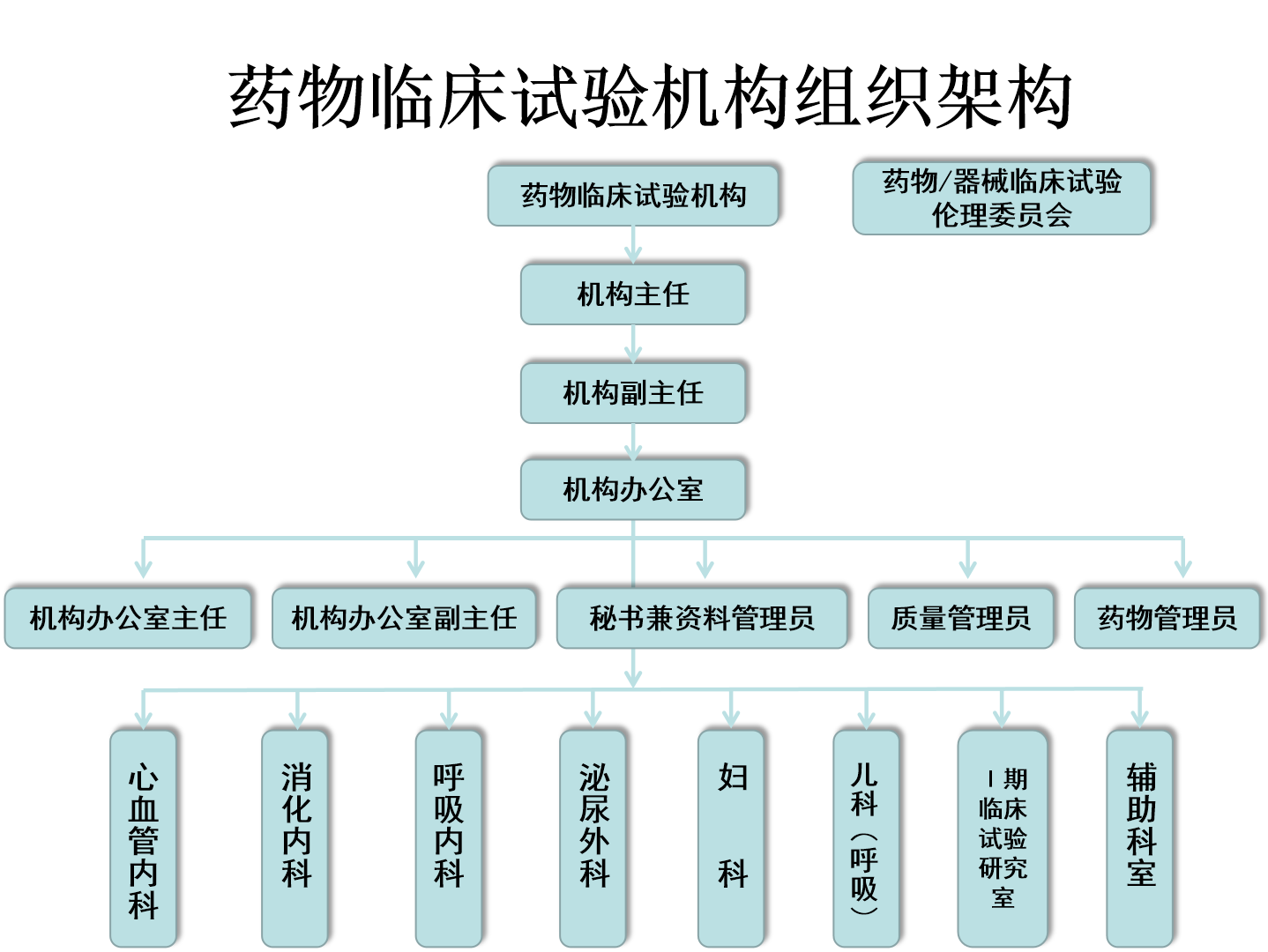
药物临床试验机构隶属于医院药剂科,由院长担任机构主任,下设机构办公室,设有机构办公室主任、机构办公室副主任、机构办公室秘书、质量管理员、资料管理员、药物管理员。机构办公室全面负责各类临床试验项目的管理,为各专业科室提供服务、监管、协调组织和培训等工作。
机构配备GCP中心药房及资料室、学术会议室。GCP中心药房配备专职药师,对试验用药品实行集中规范化管理。各专业均有用于临床试验的专科病房、专科门诊及试验所需的配套设备,以及处理严重不良事件所需的急救药品和抢救设备。此外,医技(辅助)科室(药剂科、医学检验科、超声诊断科、医学影像科等)也纳入整个临床试验管理范畴,参与临床试验工作。医务科、信息科、急救中心、重症医学科(ICU)等科室全方位提供支持,医院完善的急救体系、独立的药物/器械临床试验伦理委员会,满足开展临床试验的需求,保证临床试验在我院的顺利运行。
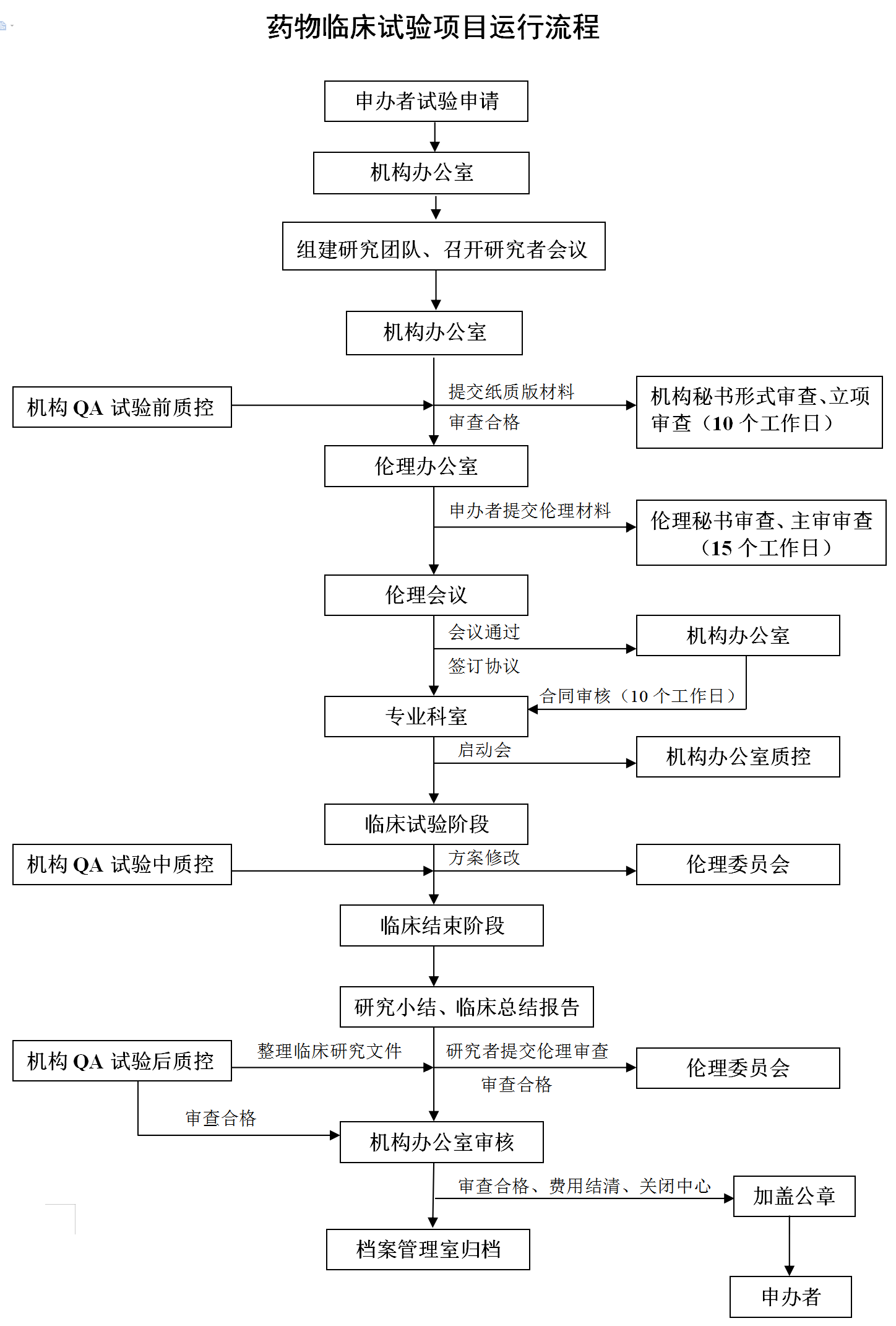
我院现有200余名研究人员通过国家级GCP培训并获得资格证书。机构按照《药物临床试验质量管理规范》要求,制定了一套系统的临床试验管理制度、标准操作规程及规范,对临床试验全过程进行管理。机构每年组织GCP法规与技术培训,加强研究者队伍建设,完善质量控制体系,保证临床试验各项目按照GCP原则和试验方案进行,保障受试者安全,保证数据的真实性,使各项临床试验项目高质量地完成。
机构可承接的临床试验包括:
1.新药Ⅰ期临床试验(药代动力学、生物等效性/生物利用度试验)
2.Ⅱ-Ⅳ期药物临床试验
2.医疗器械临床试验
3.体外诊断试剂临床试验
4.申办方或研究者发起的非注册类药物相关临床试验
联系方式:
机构办公室:覃老师 0755-85278975,15626049540,18475392977
传真:0755-85278975
地址:深圳市宝安区松岗镇沙江路2号深圳市宝安区松岗人民医院综合楼16楼
邮编:518100
2018年11月1日,我院顺利完成了国家药品监督管理局医疗器械临床试验机构备案工作(备案号:械临机构备201800376),其中16科室共32专业成功备案,基本涵盖所有可能涉及开展器械临床试验的科室,包括康复医学科、中医科、口腔科、新生儿、儿科(3个亚专业)、妇科、产科、呼吸内科、消化内科、心血管内科、泌尿外科、普通外科病理科、医学影像科、超声诊断科、医学检验科等,其中临床科室12个,医技科室4个。完成备案后,这32个专业即可与医疗器械研发机构合作,开展医疗器械临床试验。
我院将有更多的专业科室和研究人员参与医疗器械临床试验工作,同时我院临床试验机构办公室将继续严控质量,扎实工作,进一步加强临床试验机构建设,严格遵循GCP及相关法律法规,推动临床试验的依法依规、规范有序开展。
深圳市宝安区松岗人民医院医疗器械临床试验机构联系方式:
覃老师 0755-85278975,15626049540,18475392977
我院于2018年8月正式成立Ⅰ期临床试验研究室,组建一个由院领导领衔的Ⅰ期临床试验研究团队,研究团队包括专兼职医生4名,专兼职5护士,专兼职药师2名以及其他数名相关研究人员,其中博士2人,硕士4人,聘任北京大学人民医院方翼教授为Ⅰ期临床试验研究室名誉主任及学科带头人。所有专兼职工作人员均经过国家级或省级GCP相关培训,并具备相应的岗位资格。
研究室位于新住院大楼十六楼,使用面积约1100㎡,设有研究病房34张,8间临床观察室,1间抢救室,有较为完善的管理制度、标准操作规程和应急预案。设立了受试者接待室、体检筛查室、活动室、配餐室、抢救室、资料室、医生办公室、CRC/CRN办公室、样本处理室、样本储藏室、药品处理/储藏室等,同时,配备全方位监控系统、紧急呼叫系统、门禁系统,采用的电子数据信息系统集受试者筛查、人员管理、项目管理、受试者管理、样本管理和设备管理等功能于一体,使试验更加规范、高效;建立实时监控电子信息系统,对参加创新药临床试验的受试者进行动态监护,确保包括各项数据及检测结果都能溯源;使用温湿度监控系统的,使药物和样本的保存更有保障;抢救设备齐全,配有呼吸机、心电监护仪、除颤仪、吸痰器等设备,并开辟抢救绿色通道保障受试者的安全。
Ⅰ期临床试验研究室可开展仿制药质量和疗效一致性评价及创新药物临床研究工作。
Ⅰ期临床试验研究室简介